
مقدمه
سندرم آبآوردگی پریکارد و هپاتیت (Hydropericardium-hepatitis syndrome) HHS
که با نامهای بیماری آنگارا و سندرم لیچی (به دلیل شکل قلب درگیر) نیز شناخته میشود، یک بیماری عفونی و مسری ویروسی در طیور است که خسارات اقتصادی قابلتوجهی به صنعت پرورش جوجههای گوشتی در سراسر جهان وارد میکند . این بیماری با درصد ابتلا و تلفات بالا بهویژه در گلههای جوان مشخص میشود. علامت شاخص آن تجمع مایع سروزی و شفاف در کیسه پریکارد (آبآوردگی قلب) همراه با هپاتیت و کانونهای نکروز در کبد است. اگرچه سالها از شناسایی این بیماری میگذرد، اما همچنان بهعنوان یک تهدید نوپدید در بسیاری از نقاط جهان مطرح است و تحقیقات گستردهای برای شناخت ابعاد مختلف آن در حال انجام است .
تاریخچه
بیماری آنگارا برای اولین بار در سال ۱۹۸۷ در منطقه آنگارا در نزدیکی کراچی پاکستان تشخیص داده شد و به همین دلیل به این نام شهرت یافت . در آن زمان، تلفات ناگهانی و بالا در گلههای جوجههای گوشتی مشاهده شد که با علائمی مانند آبآوردگی شدید پریکارد همراه بود. به سرعت، این بیماری در مناطق با تراکم بالای مرغداری در پاکستان، مانند نزدیکی اورابان، گسترش یافت. پس از پاکستان، شیوع بیماری در سال ۱۹۸۹ در ایالت کوئرتارو مکزیک و سپس در سال ۱۹۹۰ به پنج ایالت دیگر این کشور گزارش شد. در سال ۱۹۹۴، تلفات ناشی از این سندرم در مناطق پرتراکم پرورش طیور گوشتی در دهلی نو هندوستان ظاهر گردید. متعاقباً، حضور بیماری آنگارا در کشورهای عراق، شیلی و پرو نیز تأیید شد. امروزه دامنه شیوع این بیماری فراتر رفته و به عنوان یک معضل جهانی، گزارشهایی از وقوع آن در کشورهای اروپایی و روسیه نیز منتشر شده است . مطالعات جدید در ایران نیز وقوع این سندرم را نه تنها در گلههای صنعتی، بلکه درگلههای بومی و حیاط خلوت نیز تأیید کرده است.
سببشناسی (عامل بیماری)
در ابتدا، تصور میشد که بیماری آنگارا ناشی از مسمومیت یا اختلالات تغذیهای است. با این حال، پژوهشگران با تزریق عصاره هموژن کبد پرندگان آلوده به جوجههای سالم، ماهیت عفونی عامل بیماری را اثبات کردند. مشاهده اجسام بازوفیلیک داخل هستهای در سلولهای کبدی، تلاشها برای جداسازی یک عامل ویروسی را آغاز کرد. در سال ۱۹۸۸، سرانجام مشخص شد که عامل اصلی این بیماری، آدنوویروس گروه یک (FAdV) است. امروزه تأیید شده است که سروتیپ ۴ آدنوویروس طیور (FAdV-4) عامل اصلی و اولیه این سندرم است، اگرچه گاهی سروتیپهای دیگر نظیر ۸ (DCV-94) و ۱۱ نیز در ایجاد آن نقش دارند . این ویروس نسبت به حلالهای چربی مانند اتر و کلروفرم مقاوم است و حرارت ۶۰ درجه سانتیگراد به مدت ۳۰ دقیقه آن را غیرفعال میکند. یکی از پیچیدگیهای اتیولوژی این بیماری، بحث حضور یک عامل ویروسی کمککننده (عامل اضافی) بوده است. برخی مطالعات در مکزیک (۱۹۹۴) وجود یک ویروس RNA را مطرح کردند، اما دیدگاه رایج و پذیرفتهشدهی فعلی بر این است که آدنوویروس سروتیپ ۴ به تنهایی قادر به ایجاد بیماری است، هرچند شدت و شیوع آن میتواند تحت تأثیر عفونتهای همزمان به شدت افزایش یابد .
اپیدمیولوژی و بیماریزایی
میزبان و سن حساس: میزبان اصلی این ویروس، جوجههای گوشتی جوان بهویژه در سنین ۳ تا ۶ هفتگی هستند . با این حال، مواردی از بیماری در مرغان مادر نابالغ و پولتهای تخمگذار نیز مشاهده شده است. تحقیقات جدیدتر نشان داده است که اردکهای گوشتی نیز میتوانند به این ویروس حساس باشند و علائم مشابهی را بروز دهند .
انتقال: انتقال ویروس هم به صورت عمودی (از مادر به جوجه از طریق تخممرغ) و هم به صورت افقی (از پرنده به پرنده) صورت میگیرد . ویروس در گلههای مادر تا زمان بلوغ باقی مانده و در شرایط تضعیف سیستم ایمنی یا استرس، دفع میشود. انتقال افقی عمدتاً از طریق مدفوع و ترشحات آلوده صورت میگیرد. تجهیزات، لباس و وسایل نقلیه آلوده نیز در گسترش بیماری نقش دارند. تحقیقات جدیدتر نشان میدهد که روده، اولین سد دفاعی در برابر ویروس است و ویروس پس از ورود از طریق خوراکی، سلولهای اپیتلیال روده را آلوده کرده و از این طریق وارد چرخه عفونتزایی میشود .
عوامل مستعدکننده: تراکم بالای مرغداریها، وجود گلههای با سنین مختلف در یک منطقه، عدم رعایت بهداشت، و استرسهای مدیریتی از عوامل اصلی شیوع بیماری هستند. نکته بسیار مهم، تأثیر بیماریهای تضعیفکننده سیستم ایمنی مانند بیماری گامبورو (IBD) و کمخونی عفونی جوجهها (CIA) است. عفونت همزمان با این ویروسها شدت بیماری آنگارا را به شدت افزایش داده و تلفات را تا بیش از ۸۰ درصد بالا میبرد.
علائم و نشانهها
علائم بالینی: بیماری آنگارا معمولاً با شروع ناگهانی تلفات (۵-۳ درصد در روز) در گله ظاهر میشود. پرندگان مبتلا علائم غیراختصاصی مانند بیحالی، افسردگی، جمع شدن در کنار هم، ژولیدگی پرها و اسهال مخاطی زرد رنگ را نشان میدهند.

یافتههای آزمایشگاهی: در آزمایش خون، کاهش معنیدار در سطح هموگلوبین، هماتوکریت و شمارش گلبولهای قرمز و سفید دیده میشود (کمخونی و لکوپنی). همچنین به دلیل آسیب شدید کبدی، آنزیمهای کبدی مانند لاکتات دهیدروژناز، آلکالین فسفاتاز و آلانین آمینوترانسفراز افزایش یافته و سطح پروتئین تام و آلبومین خون کاهش مییابد. این هیپوپروتئینمی عامل اصلی تجمع مایع در پریکارد محسوب میشود
یافتههای کالبدگشایی (ضایعات پس از مرگ):
– آبآوردگی پریکارد: بارزترین ضایعه، تجمع مایع ترانسودای زرد روشن و ژلاتینیشکل درون کیسه پریکارد است. گاهی حجم این مایع به بیش از ۱۰ سیسی میرسد و قلب را شبیه میوه لیچی میکند که نام دیگر بیماری نیز از همین روست .
– کبد: کبد بزرگ، رنگپریده، شکننده و ترد میشود و ممکن است خونریزیهای پتشی روی کپسول آن دیده شود.
– کلیهها: کلیهها نیز مشابه کبد، متورم و رنگپریده هستند.
– ریه: ادم ریوی و پرخونی عمومی در لاشه قابل مشاهده است.

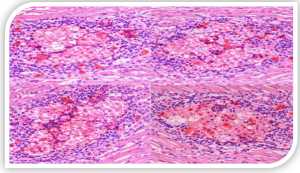
یافتههای میکروسکوپی: مهمترین ضایعه میکروسکوپی، حضور اجسام بازوفیلیک داخل هستهای در سلولهای کبدی (هپاتوسیتها) است . نکروز انعقادی
چندکانونی در کبد، دژنرسانس و نکروز سلولهای عضله قلب و توبولهای کلیوی نیز از دیگر یافتههای بافتشناسی هستند.
تشخیص
تشخیص اولیه بر اساس مشاهده علائم بالینی و ضایعات مشخص کالبدگشایی بهویژه آبآوردگی پریکارد و هپاتیت همراه با اجسام بازوفیلیک داخل هستهای در بررسیهای میکروسکوپی بافت کبد صورت میگیرد .
برای تشخیص قطعی و تایید سروتیپ ویروس، روشهای آزمایشگاهی زیر به کار میروند:
– جداسازی ویروس: تزریق سوسپانسیون کبد یا بافتهای آلوده به تخممرغ جنیندار SPF یا کشت سلولی (مانند سلولهای کبدی LMH)).
– میکروسکوپ الکترونی: برای مشاهده مستقیم ذرات ویروس.
– آزمایشات سرولوژیکی: مانند خنثیسازی سرمی (SNT)، ایمونودیفیوژن در آگار ژل (AGID) و الایزا برای شناسایی آنتیبادیها.
– روشهای مولکولی: امروزه آزمایش PCR و Real-Time PCR به عنوان روشهای سریع، حساس و اختصاصی برای تشخیص ژنوم ویروس و تعیین سروتیپ آن به طور گسترده استفاده میشوند .
درمان
تاکنون درمان اختصاصی و مؤثری برای بیماری آنگارا شناخته نشده است. استفاده از ترکیبات یددار در آب آشامیدنی (یدوفور با غلظت ۰.۱-۰.۰۷ درصد) در برخی مناطق برای کاهش تلفات تجربه شده است، اما این روش یک درمان قطعی محسوب نمیشود و مکانیسم اثر آن کاملاً مشخص نیست.
افقهای جدید درمانی: تحقیقات اخیر نویدبخش روشهای درمانی جدیدی هستند:
– اینترفرونها: مطالعات نشان داده است که اینترفرونهای نوع I (IFN-α) و III (IFN–λ) مرغی که به روش نوترکیب تولید شدهاند، توانایی مهار تکثیر ویروس FAdV-4 را در شرایط آزمایشگاهی دارند. این ترکیبات با تحریک بیان ژنهای محرک اینترفرون (ISGs) از مراحل مختلف چرخه زندگی ویروس جلوگیری میکنند .
– کامپتوتسین: در پژوهشی در سال ۲۰۲۲، نشان داده شد که ترکیب کامپتوتسین (Camptothecin) با مسدود کردن مرحله تکثیر ویروس در سلول، اثر ضدویروسی قابل توجهی علیه FAdV–4 داشته و در مدل حیوانی باعث افزایش میزان بقای جوجههای آلوده شده است. اگرچه این یافتهها در مراحل اولیه تحقیقاتی هستند، اما میتوانند در آینده به تولید داروهای مؤثری برای کنترل بیماری منجر شوند.
پیشگیری و کنترل
با توجه به عدم وجود درمان اختصاصی، پیشگیری و کنترل بیماری آنگارا بر سه محور اصلی استوار است:
۱. امنیت زیستی: رعایت اصول بهداشتی، مهمترین و اولین خط دفاعی است. این اقدامات شامل موارد زیر است:
– ایجاد فاصله حداقل ۲ کیلومتری بین فارمهای صنعتی.
(All-in All-out) – اجرای سیستم تمامدر تمامخارج در پرورش.
– جلوگیری از ورود افراد، تجهیزات و وسایل نقلیه آلوده به فارم.
– ضدعفونی مؤثر آب آشامیدنی و محیط.
– کنترل جوندگان و پرندگان وحشی.
۲. واکسیناسیون: مؤثرترین راهبرد کنترلی در مناطق اندمیک، واکسیناسیون است.
– واکسن کشته: در پاکستان و هند، واکسن غیرفعال تهیه شده از عصاره کبد جوجههای SPF آلوده (غیرفعال شده با فرمالین) با موفقیت در کاهش تلفات گلههای گوشتی به کار گرفته شده است .
– واکسن روغنی: در مکزیک، واکسن غیرفعال فرمالینه در امولسیون روغنی توانسته است محافظت ۱۰۰ درصدی در گلههای در معرض بیماری ایجاد کند.
– پیشرفتهای جدید واکسن: تحقیقات کنونی بر روی تولید واکسنهای زیرواحد نوترکیب و واکسنهای کایمریک متمرکز شده است. به عنوان مثال، واکسنی که حاوی پروتئین فیبر کایمریک (ترکیبی از سروتیپهای ۴ و ۸ یا ۱۱) است، میتواند همزمان پرندگان را در برابر HHS و هپاتیت با اجسام اینکلوزیون (IBH) محافظت کند .
۳. مدیریت گلههای مادر: ایمنسازی گلههای مادر قبل از دوره تخمگذاری از طریق واکسیناسیون، میتواند آنتیبادیهای مادری را به نتاج منتقل کرده و جوجهها را در روزهای اول زندگی در برابر عفونت محافظت نماید.
نتیجهگیری
بیماری آنگارا (سندرم آبآوردگی پریکارد و هپاتیت) یک تهدید جدی و مداوم برای صنعت طیور بهویژه در مناطقی با تراکم بالای پرورش جوجههای گوشتی است. اگرچه عامل بیماری (آدنوویروس سروتیپ ۴) به خوبی شناخته شده است، اما تعامل آن با سایر عوامل تضعیفکننده ایمنی، پیچیدگیهای خاصی در کنترل بیماری ایجاد میکند. تشخیص سریع و دقیق با استفاده از روشهای مولکولی مدرن، کلید مهار بهموقع کانونهای بیماری است. با توجه به محدودیتهای درمانی، استراتژیهای کنترلی باید بر تقویت امنیت زیستی و اجرای برنامههای واکسیناسیون کارآمد با استفاده از واکسنهای نسل جدید متمرکز باشد. تحقیقات آینده در زمینه تولید داروهای ضدویروسی و واکسنهای نوترکیب چندظرفیتی، نویدبخش کنترل مؤثرتر این بیماری و کاهش خسارات ناشی از آن در سراسر جهان است.
منابع
بیشتر یاد بگیرید